A | B | C | D |
|
|
|
|
冰墩墩中的聚酯纤维 | 速滑馆中的铝制幕墙 | 雪花花瓣中的聚碳酸酯 | 头盔表面的聚氨酯涂料 |

下列说法正确的是( ___ )
A | B | C | D |
|
|
|  |
实验室制取氨气 | 分离碳酸钠溶液和乙酸乙酯 | 制备无水氯化镁 | 证明醋酸为弱酸 |
下列说法不正确的是( ___ )

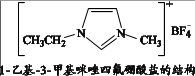
已知:参与原电池反应的氧化剂(还原剂)氧化性(还原性)越强,原电池的电压越大。
下列说法不正确的是( ___ )
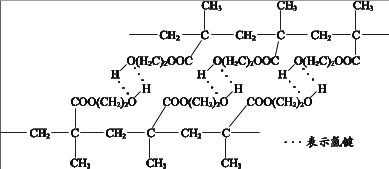
下列关于该高分子说法不正确的是( ___ )
已知:2KMnO4 + 16HCl = 2KCl + 5Cl2↑ + 2MnCl2 + 8H2O
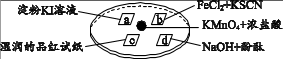
下列对“实验现象”的“解释或结论”描述,不正确的是( ___ )
选项 | 实验现象 | 解释或结论 |
A | a处试纸变蓝 | 氧化性:Cl2 > I2 |
B | b处试纸变红 | Cl2 + 2Fe2+ = 2Cl- + 2Fe3+ |
C | c处试纸褪色 | Cl2与H2O反应生成了具有漂白性的物质 |
D | d处红色褪去 | Cl2 和NaOH反应使溶液呈中性 |
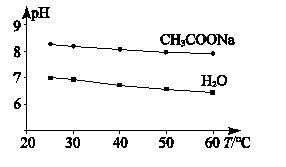
下列说法不正确的是( ___ )
已知:Cr2O72-(橙) + H2O 2 CrO42-(黄) + 2 H+
下列对实验过程的分析中,不正确的是( ___ )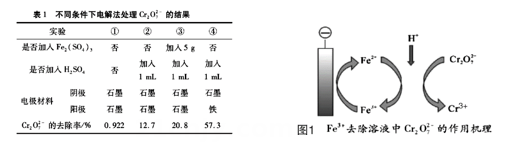
回答下列问题。
反应i.CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H1
反应ii.CO2(g) + H2(g) CO(g) + H2O(g) △H2= + 41.2 kJ·mol-1
回答下列问题。

已知: ![]()
回答下列问题。
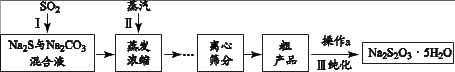
资料:① Na2S2O3 • 5H2O无色、易溶于水,难溶于乙醇;
② Na2S2O3在酸性溶液中反应有S和SO2产生
(一)制备
工业上可用SO2、Na2S和 Na2CO3制备Na2S2O3 • 5H2O,其工艺流程示意图如下: