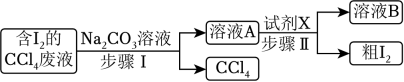
| 材料 | 组成和结构变化 | 性能变化 |
A | 生铁 | 减少含碳量 | 延展性增强 |
B | 晶体硅 | 用碳原子取代部分硅原子 | 导电性增强 |
C | 纤维素 | 接入带有强亲水基团的支链 | 吸水能力提高 |
D | 顺丁橡胶硫 | 硫化使其结构由线型转变为网状 | 强度提高 |
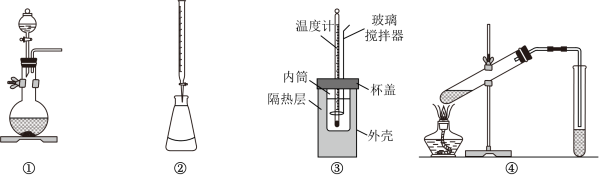
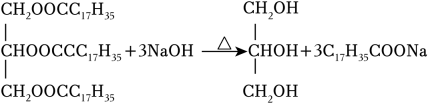

下列说法不正确的是( )
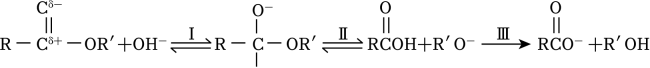
已知:
①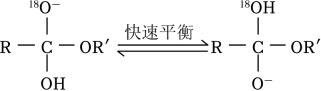
②RCOOCH2CH3水解相对速率与取代基R的关系如下表:
取代基R | CH3 | ClCH2 | Cl2CH |
水解相对速率 | 1 | 290 | 7200 |
下列说法不正确的是( )
已知:H2SO3 Ka1=1.4×10﹣2 , Ka2=6.0×10﹣8。Ksp(BaSO3)=5.0×10﹣10 , Ksp(BaSO4)=1.1×10﹣10。
下列说法不正确的是( )
| 实验目的 | 方案设计 | 现象 | 结论 |
A | 探究Cu和浓HNO3反应后溶液呈绿色的原因 | 将NO2通入下列溶液至饱和: ①浓HNO3 ②Cu(NO3)2和HNO3混合溶液 | ①无色变黄色 ②蓝色变绿色 | Cu和浓HNO3反应后溶液呈绿色的主要原因是溶有NO2 |
B | 比较F﹣与SCN﹣结合Fe3+的能力 | 向等物质的量浓度的KF和KSCN混合溶液中滴加几滴FeCl3溶液,振荡 | 溶液颜色无明显变化 | 结合Fe3+的能力:F﹣>SCN﹣ |
C | 比较HF与H2SO3的酸性 | 分别测定等物质的量浓度的NH4F与(NH4)2SO3溶液的pH | 前者pH小 | 酸性:HF>H2SO3 |
D | 探究温度对反应速率的影响 | 等体积、等物质的量浓度的Na2S2O3与H2SO4溶液在不同温度下反应 | 温度高的溶液中先出现浑浊 | 温度升高,该反应速率加快 |
已知: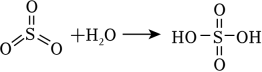
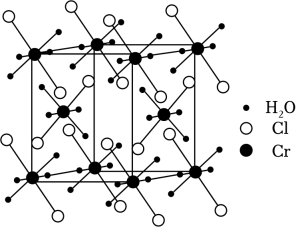
请回答:
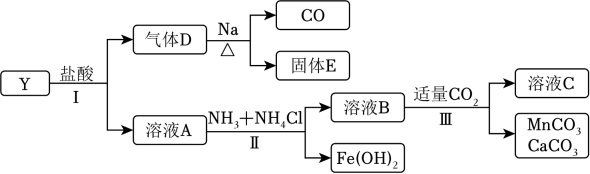
已知:NH3与溶液A中金属离子均不能形成配合物。
请回答:
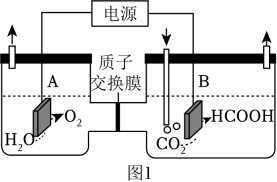
请回答:
已知:①H2S的沸点是61℃,有毒:
②装置A内产生的H2S气体中含有酸性气体杂质。
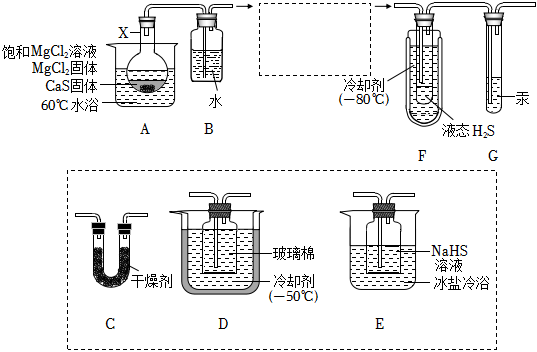
请回答:
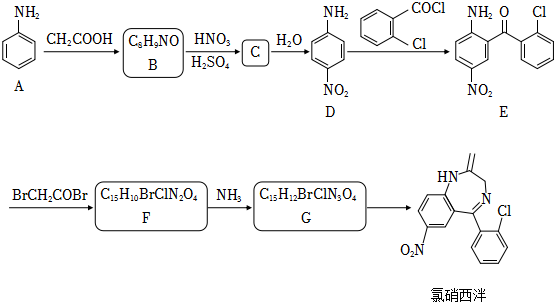
已知:
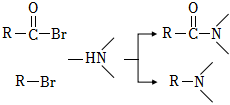
请回答: