B.
B. 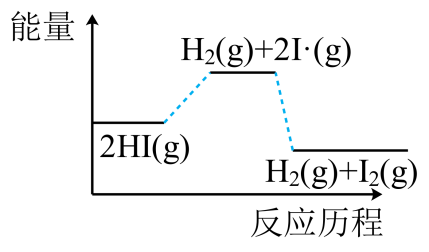 C.
C. 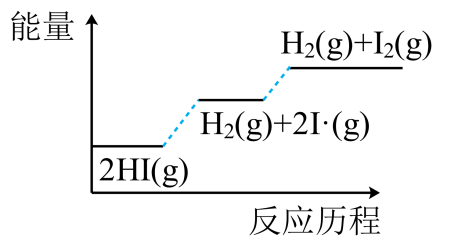 D.
D. 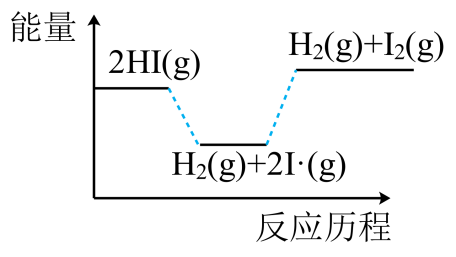
化学键 | ||||
1 | x | 498 | 803 | 464 |
下列说法正确的是( ___ )
|
|
|
|
① | ② | ③ | ④ |
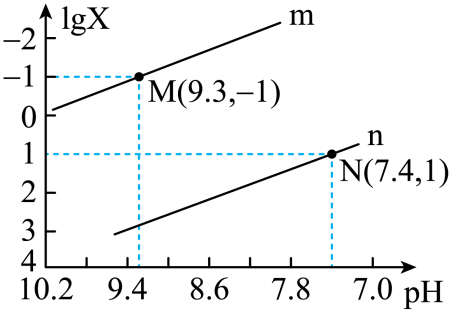
弱酸 | HCOOH(甲酸) | HClO | ||
K(25℃) |
|
|
|
|
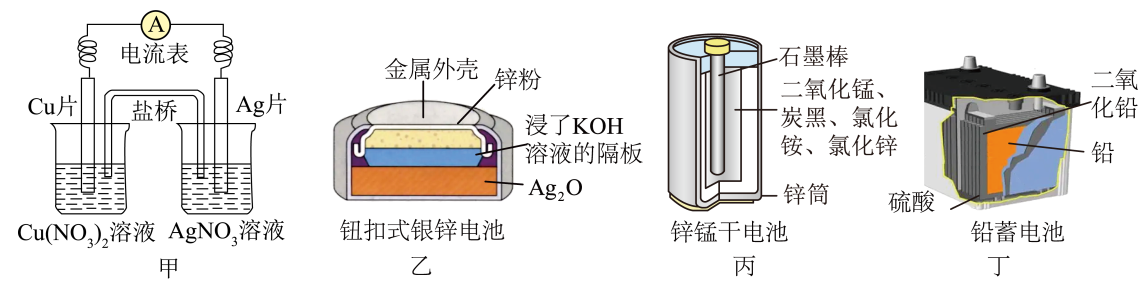
A.排出酸式滴定管中的气泡 | B.灼烧海带 | C.比较CH3COOH的Ka和H2CO3的Ka1大小 | D.测定氯水的pH |
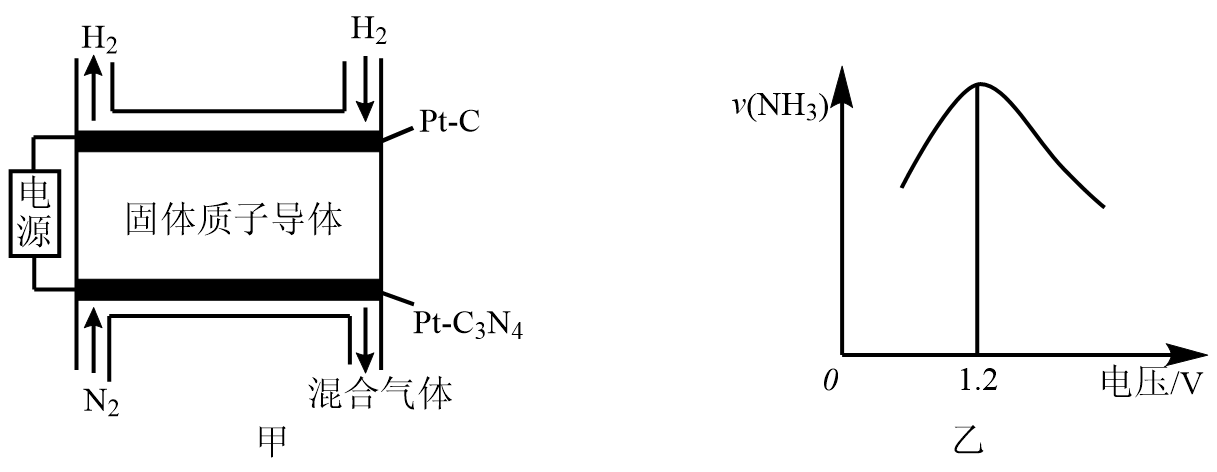
①4NH3(g)+5O2(g)4NO(g)+6H2O(g) △H1
②4NH3(g)+3O2(g)2N2(g)+6H2O(g) △H2
下列说法正确的是( ___ )
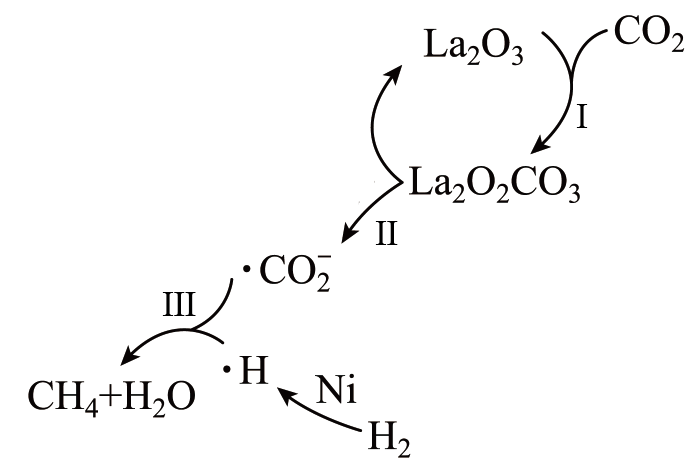
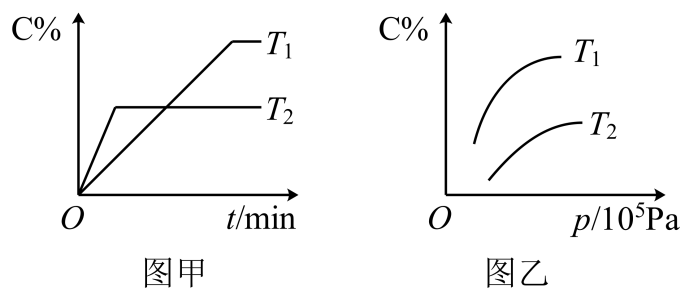
①CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1
②CO2(g)+H2(g)CO(g)+H2O(g) △H2=+41.2kJ•mol-1
其他条件不变,在相同时间内温度对CO2催化加氢的影响如图。下列说法不正确的是( ___ )

已知:CH3OH的选择性=×100%